Lecanemab được bán trên thị trường với tên Leqembi, là phương pháp điều trị đầu tiên được chứng minh là làm chậm sự tiến triển của bệnh Alzheimer. Loại thuốc này dự kiến sẽ được bảo hiểm y tế công cộng chi trả, mở đường cho việc sử dụng rộng rãi hơn.
Dược phẩm sinh học làm giảm các mảng amyloid beta - một loại protein tích tụ trong não của những người mắc bệnh Alzheimer. Trong một thử nghiệm lâm sàng có kết quả được công bố vào năm 2022, lecanemab đã được chứng minh là làm chậm 27% tốc độ suy giảm nhận thức.
Teresa Buracchio, Giám đốc Văn phòng Khoa học thần kinh tại Trung tâm đánh giá và nghiên cứu thuốc của FDA cho biết: "Việc phê duyệt này là minh chứng cho thấy lợi ích lâm sàng đối với căn bệnh tàn khốc này, điều này có ý nghĩa rất to lớn đối với người bạn và gia đình họ".
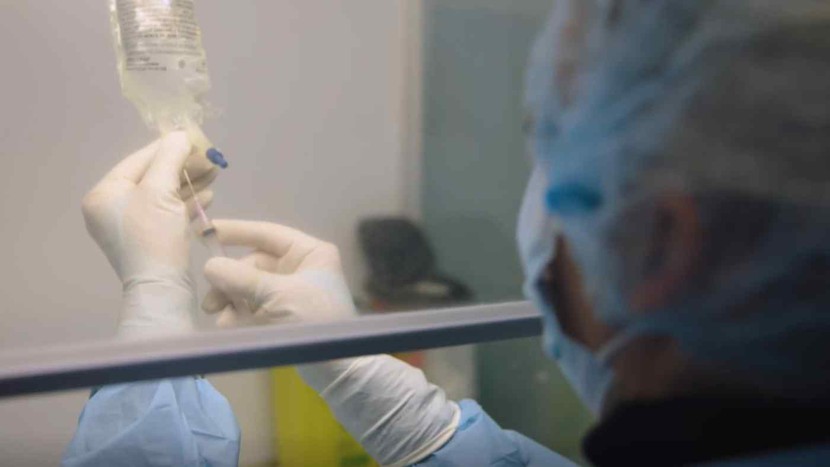
Lecanemab được dùng cho bệnh nhân trong một thử nghiệm lâm sàng ở Mỹ. Ảnh: Eisai
Trước đó vào tháng 1, FDA đã bật đèn xanh tạm thời cho loại thuốc này theo lộ trình phê duyệt nhanh. Eisai và Biogen đã đệ trình lecanemab để phê duyệt chính thức, nhận được sự chấp thuận nhất trí từ ban cố vấn của FDA vào tháng trước.
Bệnh Alzheimer chiếm 60% đến 70% bệnh nhân sa sút trí tuệ. Theo tổ chức phi lợi nhuận Alzheimer's Disease International, số người mắc chứng mất trí nhớ dự kiến sẽ tăng từ 50 triệu bệnh nhân hiện tại lên 150 triệu bệnh nhân vào năm 2050.
Hiện tại, có hơn 6 triệu bệnh nhân ở Mỹ và 5-6 triệu bệnh nhân ở Nhật Bản.
Trung tâm Dịch vụ Medicare và Medicaid của Mỹ, cơ quan quản lý bảo hiểm y tế công cho người cao tuổi, đã thông báo vào tháng 1 rằng lecanemab sẽ được bảo hiểm rộng rãi nếu FDA chính thức phê duyệt thuốc này.
(Nguồn: Nikkei Asia)









Cùng chuyên mục
Woman Vietnam và nỗ lực thích nghi với xu hướng tiêu thụ tin tức qua video ngắn của thế hệ trẻ
Yến sào Khánh Hòa doanh thu tăng vượt cùng kỳ, xuất khẩu Hoa Kỳ thành công lô hàng nước giải khát Sana đầu tiên
Xe Sài Gòn - Thuê xe 16 chỗ đi Vũng Tàu tiện lợi cho mọi chuyến đi
Cú xoay trục của Masan: Tăng trưởng ba chữ số, WinCommerce đổi vận sau tái cấu trúc
Chủ động chăm sóc sức khỏe gia đình dễ dàng hơn với Vietnam Health News
Hoa tươi Hoa Thị - Nơi hoa nói thay lời yêu thương