Trong thông báo, Moderna cho biết công ty sẽ đệ đơn xin cấp phép lên Cơ quan cấp phép sử dụng khẩn cấp (EUA) thuộc Cơ quan quản lý thực phẩm và dược phẩm Mỹ (FDA). Thông báo cũng nêu rõ Moderna sẽ xin cấp phép "tiếp thị có điều kiện" với Cơ quan Dược phẩm châu Âu (EMA).
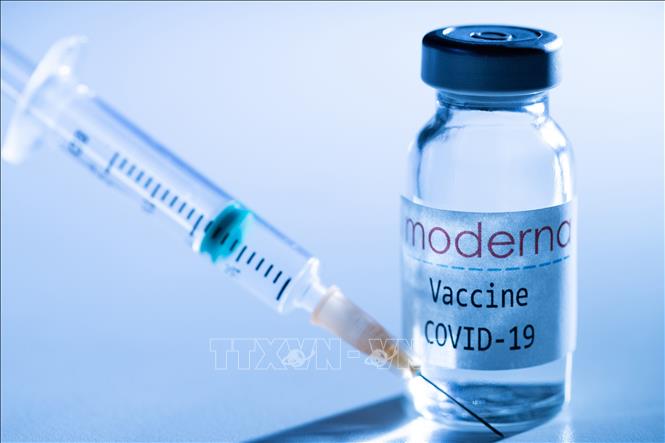 |
| Vaccine ngừa COVID-19 của hãng dược phẩm Mỹ Moderna. Ảnh: AFP/TTXVN |
Trước đó, Moderna thông báo kết quả đầy đủ thử nghiệm giai đoạn cuối vaccine COVID -19 của hãng cho hiệu quả 94,1%, không gây nguy cơ nghiêm trọng và tỷ lệ hiệu quả khá đồng đều giữa các nhóm tuổi, chủng tộc, sắc tộc và giới tính. Vaccine của Moderna còn được cho là có tỷ lệ 100% ngăn chặn thành công các ca bệnh nặng. Cụ thể, trong số 196 tình nguyện viên mắc COVID-19 trên tổng số hơn 30.000 người tham gia thử nghiệm, có 185 người dùng giả dược và chỉ có 11 người dùng vaccine. Trong số 196 ca bệnh, có 30 ca mắc bệnh nặng và đều thuộc nhóm dùng giả dược- đồng nghĩa với hiệu quả ngăn chặn các ca bệnh nặng của vaccine là 100%.
Moderna cho biết đang trong lộ trình sản xuất khoảng 20 triệu liều vaccine sẵn sàng bàn giao cho Mỹ vào cuối năm 2020 và đủ để chủng ngừa cho 10 triệu người dân nước này. Bên cạnh việc xin cấp phép tại Mỹ, Moderna cũng sẽ xin EMA cấp phép "có điều kiện đi kèm". Mới đây, EMA đã triển khai quá trình đánh giá "cuốn chiếu" với các dữ liệu về vaccine của Moderna để đẩy nhanh tiến trình cấp phép và sẽ tiếp tục đàm phán với các cơ quan quản lý khác.
Như vậy, vaccine của Moderna là loại thứ 2 có thể được giới chức Mỹ cấp phép sử dụng khẩn cấp trong năm nay, sau vaccine của Pfizer và BioNTech cho hiệu quả thử nghiệm 95%. Trước đó khoảng một tuần, Pfizer đã xin cấp phép sử dụng khẩn cấp tại Mỹ và châu Âu.
Trong khi đó, Nga cũng bắt đầu đưa loại vaccine phòng COVID-19 thứ 2 tại quốc gia này vào thử nghiệm lâm sàng quy mô lớn với người trên 18 tuổi từ ngày 30/11. Hãng tin RIA dẫn nguồn tin từ Cơ quan quản lý y tế Rospotrebnadzo cho biết vaccine EpiVacCorona do viện Vector ở Siberia phát triển và trong tháng này mới được cấp phép đưa vào thử nghiệm với 150 tình nguyện viên trên 60 tuổi và 3.000 tình nguyện viên trên 18 tuổi.
Hãng tin TASS cho biết các thử nghiệm sẽ được tiến hành tại Moskva và một số thành phố khác, trong đó có Kazan và Kaliningrad. Hồi đầu tháng này Nga cũng thông báo vaccine phòng COVID-19 có tên gọi Sputnik V do nước này phát triển cho hiệu quả phòng bệnh lên tới 92% trong thử nghiệm lâm sàng.
Công ty sản xuất vaccine Novavax Inc (Mỹ) thông báo tiếp tục hoãn thử nghiệm lâm sàng quy mô lớn với vaccine COVID-19 của hãng tại Mỹ và hy vọng có thể triển khai kế hoạch này trong những tuần tới. Đây là lần thứ 2 Novavax phải hoãn kế hoạch thử nghiệm giai đoạn 3 vaccine COVID-19 tại Mỹ. Kế hoạch ban đầu là vào tháng 10 vừa qua.
Lý do chủ yếu là hãng không thể đẩy mạnh năng lực sản xuất vaccine. Novavax có kế hoạch sử dụng các nguyên liệu vaccine được sản xuất theo quy mô thương mại để thử nghiệm tại Mỹ và Mexico và cũng đã làm việc chặt chẽ với FDA để được cấp phép sử dụng vaccine tại nhà máy ở North Carolina.
Hiện hãng đang tiến hành thử nghiệm trên diện rộng tại Anh với khoảng 15.000 người tham gia và hy vọng sẽ có dữ liệu sơ bộ trong khoảng quý I/2020. Trước đó, hãng cho biết thử nghiệm tại Anh có thể được làm cở sở để xin cấp phép tại nhiều quốc gia.
(TTXVN)












Cùng chuyên mục
Lộ loạt chế độ giảm cân gây sốc của idol: Ăn 1 quả táo mỗi ngày, chỉ ăn đá lạnh suốt cả tuần
Người Nhật không để mét vuông nào trong nhà bị lãng phí: Có 5 thiết kế đáng học hỏi, càng dùng càng thấy hợp lý
4 loại rau củ mùa hè dễ "ngậm" hóa chất nhất chợ, đặc biệt là món đầu tiên!
Người đàn ông 35 tuổi bị suy thận, bác sĩ thở dài: "Ngày nào cũng làm 2 việc này, thận khỏe đến đâu cũng khó chịu nổi"
Nghịch lý của 30s đi xin việc: Kinh nghiệm 10 năm, vẫn phải chứng minh mình “còn trẻ” ư?
Có nên bán vàng lấy tiền gửi ngân hàng?