Mới đây Bộ KH&CN đã có tin đính chính liên quan đến thông tin Tổ chức Y tế Thế giới (WHO) chấp thuận kit xét nghiệm của Công ty cổ phần Công nghệ Việt Á trên website của Bộ.
Cụ thể, Bộ KH&CN cho biết, trên cơ sở tổng hợp nguồn tin từ các cơ quan báo chí chính thống, vào lúc 15:36 ngày 26/4/2020, bản tin “Bộ kit xét nghiệm Covid-19 của Việt Nam sản xuất vừa được Tổ chức y tế thế giới chấp thuận” đã được đăng tải trên Cổng thông tin của Bộ KH&CN tại địa chỉ www.most.gov.vn.
Bản tin này đã được gửi tới một số phóng viên theo dõi lĩnh vực KH&CN tham khảo như thông lệ. Tuy nhiên, sau khi phát hiện có sai sót, để có thời gian xem xét, đánh giá lại toàn bộ quá trình, bản tin đã được tạm gỡ trên Cổng thông tin của Bộ KH&CN.
 |
| Bản tin đính chính việc kit xét nghiệm của Công ty Việt Á được WHO chấp thuận đăng trên Cổng thông tin điện tử Bộ KH&CN. |
Các đơn vị chức năng có liên quan đã kiểm tra lại và nhận thấy có sự sai sót trong quá trình tổng hợp, biên tập, kiểm chứng thông tin và cung cấp thông tin để đăng trên Cổng thông tin của Bộ.
Chính vì vậy, Bộ KH&CN đính chính lại thông tin từng được đăng tải thành: “Ngày 24/4/2020, Tổ chức Y tế thế giới (WHO) chấp thuận yêu cầu xin đánh giá sử dụng khẩn cấp (EUL) cho bộ kit “LightPower iVA SAR-CoV-2 1st RT-rPCR Kit” của Công ty cổ phần công nghệ Việt Á”.
Trước đó, vào hồi 14h54 phút ngày 26/4/2020, Trung tâm Nghiên cứu & Phát triển Truyền thông KH&CN (thuộc Bộ KH&CN) đã phát đi thông tin về việc “Bộ kit xét nghiệm Covid-19 do Việt Nam sản xuất vừa được Tổ chức y tế thế giới chấp thuận.”, trong đó nêu rõ: “Bộ Khoa học & Công nghệ cho biết, WHO đã công nhận bộ kit xét nghiệm Covid-19 của Việt Nam do Bộ Khoa học & Công nghệ giao cho Học viện Quân y và Công ty Việt Á phối hợp nghiên cứu và sản xuất.”
Thông tin này cũng được đăng tải trên website của Bộ KH&CN trong hơn 1 năm qua, từ tháng 4/2020 cho đến tháng 12/2021.
Mới đây, Văn phòng đại diện Tổ chức Y tế thế giới tại Việt Nam cũng cho biết sản phẩm LightPower iVASARS-CoV-2 1stRT-rPCR Kit của công ty Việt Á không thuộc danh sách chấp thuận thông qua quy trình EUL của WHO. Sản phẩm này đã nộp hồ sơ cho chẩn đoán in vitro Covid-19 của WHO EUL với mã hồ sơ đăng ký EUL là “EUL 0524-210-00”.
“Hồ sơ sản phẩm đã được đánh giá và không đáp ứng được các hồ sơ cần thiết về an toàn, công năng”, WHO nhấn mạnh.
Ông Trịnh Thanh Hùng, Phó vụ trưởng Vụ Khoa học và Công nghệ các khối ngành Kinh tế - Kỹ thuật, Bộ Khoa học và Công nghệ, thừa nhận đây là sơ suất của Bộ.
"Bộ chưa xem xét kỹ lưỡng thông tin phản hồi của WHO về bộ kit test của Công ty Việt Á. Thực chất WHO mới chỉ "chấp thuận đưa kit test này vào quy trình đánh giá xem xét sử dụng" không phải chấp thuận sử dụng", theo lời ông Hùng.






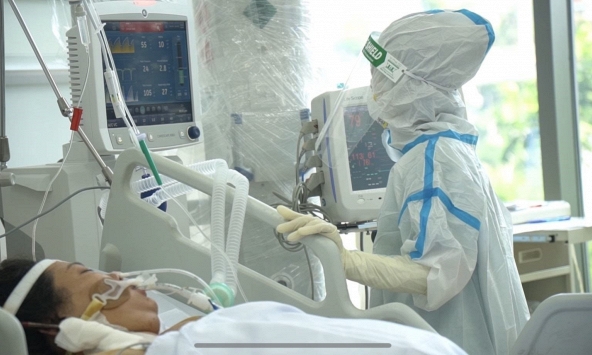












COVID-19 có thể tồn tại trong cơ thể người nhiều tháng
Đại dịch COVID-19 đã 'bần cùng' hóa gần 100 triệu người trên toàn cầu
Xuất khẩu tiêu dẫn đầu nhóm nông nghiệp trong năm 2021
Giá thủy, hải sản vẫn ổn định mặc dù không xuất được sang Trung Quốc
Thị trường chứng khoán Mỹ đóng cửa ở mức cao kỷ lục lần thứ 69 trong năm
Tử vi hàng ngày 29/12 của 12 con giáp đầy đủ, chi tiết
Cùng chuyên mục
Việt Nam – Pháp thúc đẩy hợp tác khoa học, công nghệ, đổi mới sáng tạo theo lộ trình mới
Sát ngày kick-off, Vinhomes Hải Vân Bay hút mạnh sự quan tâm nhờ hệ sinh thái sống, nghỉ dưỡng hiếm có
Vingroup khai giảng khóa đầu tiên chương trình đào tạo 20.000 nhân tài ai thực chiến
Doanh thu ngành khoa học và công nghệ tăng mạnh, thúc đẩy rà soát công nghệ chiến lược
Can thiệp mạch vành ít cản quang cứu bệnh nhân 75 tuổi suy thận nặng
Phú Quốc sắp có tuyến tàu LRT 18 phút nối sân bay với trung tâm APEC