Trong lĩnh vực y khoa, dược phẩm, dinh dưỡng và thực phẩm chức năng, các "nghiên cứu lâm sàng" và "thử nghiệm lâm sàng" có vai trò then chốt, là bằng chứng khoa học không thể thiếu để khẳng định tính an toàn, hiệu quả và giá trị của các sản phẩm chăm sóc sức khỏe. Mặc dù thường được sử dụng thay thế cho nhau, hai thuật ngữ này có những sắc thái riêng biệt và cùng tạo nên một bức tranh tổng thể về quá trình phát triển sản phẩm.
 |
Khái niệm cơ bản:
- Nghiên cứu lâm sàng (Clinical Research) là một thuật ngữ rộng, bao gồm mọi nghiên cứu khoa học trên con người hoặc dữ liệu sức khỏe của con người nhằm khám phá, xác minh hoặc đánh giá các phương pháp điều trị, chẩn đoán, hoặc phòng ngừa bệnh tật. Mục tiêu chính là nâng cao kiến thức y học và cải thiện sức khỏe cộng đồng.
- Thử nghiệm lâm sàng (Clinical Trial) là một loại hình cụ thể của nghiên cứu lâm sàng. Đây là một nghiên cứu can thiệp, được thiết kế có hệ thống để kiểm tra hiệu quả và an toàn của một phương pháp điều trị, một loại thuốc, vắc-xin, thiết bị y tế, hoặc thậm chí là một can thiệp dinh dưỡng mới trên nhóm người tình nguyện. Thử nghiệm lâm sàng thường được tiến hành qua nhiều pha (Pha I, II, III, IV) với mục tiêu và đối tượng nghiên cứu khác nhau ở mỗi pha.
Vai trò và ý nghĩa trong đánh giá sản phẩm y dược, dinh dưỡng:
- Xác minh tính An toàn: Đây là yếu tố tiên quyết. Nghiên cứu lâm sàng giúp phát hiện các tác dụng phụ, phản ứng có hại của sản phẩm, liều lượng an toàn tối đa và các đối tượng có nguy cơ đặc biệt. Với sản phẩm y dược, điều này cực kỳ quan trọng để tránh gây hại cho bệnh nhân. Với sản phẩm dinh dưỡng, dù được coi là an toàn hơn, vẫn cần xác định các tác dụng không mong muốn hoặc tương tác với cơ thể.
- Đánh giá Hiệu quả: Nghiên cứu lâm sàng cung cấp bằng chứng định lượng về khả năng của sản phẩm trong việc đạt được mục tiêu điều trị, phòng ngừa hoặc cải thiện tình trạng sức khỏe. Ví dụ như vắc-xin có tạo ra miễn dịch bảo vệ không? Hay đối với các sản phẩm dinh dưỡng, thực phảm chức năng, bằng chứng lâm sàng giúp phân biệt sản phẩm thực sự hiệu quả với những tuyên bố thiếu cơ sở như sản phẩm dinh dưỡng có thực sự tăng cường miễn dịch, cải thiện hấp thu, hỗ trợ phát triển thể chất hay giảm nguy cơ bệnh lý như quảng cáo không?
- Xác định Liều lượng và Cách sử dụng tối ưu: Thông qua các pha nghiên cứu, các nhà khoa học xác định được liều lượng phù hợp nhất, đường dùng, tần suất sử dụng để đạt hiệu quả cao nhất mà vẫn đảm bảo an toàn.
- So sánh với các phương pháp hiện có: Nghiên cứu lâm sàng thường so sánh sản phẩm mới với các phương pháp điều trị tiêu chuẩn hiện hành (standard of care) hoặc giả dược (placebo) để chứng minh tính ưu việt hoặc ít nhất là không kém hơn.
- Cơ sở cho việc Cấp phép và Lưu hành: Đây là yếu tố bắt buộc. Các cơ quan quản lý y tế trên thế giới và tại Việt Nam đều yêu cầu dữ liệu thử nghiệm lâm sàng toàn diện trước khi cấp phép lưu hành cho thuốc, vắc-xin, thiết bị y tế mới. Với thực phẩm chức năng, các nghiên cứu này cũng là cơ sở để cơ quan quản lý xác nhận các công bố về công dụng.
- Nâng cao Kiến thức Khoa học và Thực hành Y khoa: Kết quả từ các nghiên cứu lâm sàng được công bố trên các tạp chí khoa học uy tín, góp phần vào kho tàng kiến thức y học toàn cầu, định hình các phác đồ điều trị và hướng dẫn lâm sàng.
Quy trình phê duyệt Nghiên cứu Lâm sàng tại Việt Nam
Quy trình phê duyệt một nghiên cứu/thử nghiệm lâm sàng tại Việt Nam được quản lý chặt chẽ bởi các quy định của Nhà nước nhằm đảm bảo tính khoa học, đạo đức và an toàn cho người tham gia. Các văn bản pháp luật chính điều chỉnh lĩnh vực này bao gồm:
- Luật Dược số 105/2016/QH13 ngày 06/4/2016.
- Nghị định số 96/2023/NĐ-CP ngày 29/12/2023 của Chính phủ quy định chi tiết một số điều của Luật Dược và Luật sửa đổi, bổ sung một số điều của Luật Dược về thử thuốc trên lâm sàng và hậu mãi. (Nghị định này thay thế Nghị định số 54/2017/NĐ-CP và có hiệu lực từ 01/01/2024).
- Thông tư số 29/2018/TT-BYT ngày 29/10/2018 của Bộ Y tế quy định thực hành tốt thử thuốc trên lâm sàng.
- Đối với sản phẩm dinh dưỡng (thực phẩm bảo vệ sức khỏe/thực phẩm chức năng), còn có các quy định liên quan trong Luật An toàn thực phẩm và các Nghị định, Thông tư hướng dẫn của Bộ Y tế về quản lý thực phẩm chức năng
- Quy trình phê duyệt và thực hiện nghiên cứu/thử nghiệm lâm sàng tại Việt Nam được tiến hành qua các bước chặt chẽ nhằm đảm bảo tính khoa học, đạo đức và an toàn.
- Chuẩn bị Hồ sơ Đăng ký: Bước đầu tiên yêu cầu chuẩn bị một bộ hồ sơ đầy đủ, bao gồm đơn đề nghị, đề cương nghiên cứu chi tiết tuân thủ GCP (Thực hành lâm sàng tốt), hồ sơ về sản phẩm nghiên cứu (thuốc/thực phẩm chức năng/can thiệp dinh dưỡng), thông tin về nhà tài trợ, đơn vị và nghiên cứu viên chính. Đặc biệt, hồ sơ phải có bảo hiểm bắt buộc cho người tham gia, thông tin đồng thuận và phê duyệt đạo đức từ Hội đồng Đạo đức cấp cơ sở.
- Thẩm định Đạo đức và Khoa học tại Cơ sở nghiên cứu: Hội đồng Đạo đức (IRB/EC) tại các bệnh viện hoặc viện nghiên cứu sẽ tiến hành thẩm định kỹ lưỡng đề cương về cả khía cạnh đạo đức (bảo vệ quyền lợi, an toàn người tham gia) và khoa học (tính hợp lý, khả thi), sau đó đưa ra quyết định phê duyệt về mặt đạo đức.
- Nộp Hồ sơ lên Cơ quan Quản lý Nhà nước (Bộ Y tế): Hồ sơ hoàn chỉnh, kèm theo quyết định phê duyệt đạo đức từ cơ sở, sẽ được nộp lên Cục Khoa học Công nghệ và Đào tạo (đối với thuốc) hoặc Cục An toàn thực phẩm (đối với thực phẩm chức năng) thuộc Bộ Y tế. Tại đây, Bộ Y tế sẽ thành lập Hội đồng Đạo đức Quốc gia và/hoặc Hội đồng Khoa học để thẩm định lần hai ở cấp cao hơn.
- Thẩm định của Bộ Y tế: Các Hội đồng này sẽ xem xét lại toàn bộ đề cương, đặc biệt chú trọng tính đạo đức và khoa học, thiết kế nghiên cứu, và đưa ra kết luận đồng ý, không đồng ý, hoặc yêu cầu chỉnh sửa.
- Quyết định Phê duyệt: Dựa trên kết quả thẩm định, Bộ trưởng Bộ Y tế (hoặc Cục trưởng được ủy quyền) sẽ ban hành Quyết định chính thức phê duyệt hoặc từ chối thử nghiệm lâm sàng, trong đó quy định rõ phạm vi, thời gian, địa điểm và các điều kiện thực hiện.
- Thực hiện và Báo cáo: Sau khi được phê duyệt, nghiên cứu sẽ được tiến hành theo đúng đề cương. Nghiên cứu viên và nhà tài trợ có trách nhiệm báo cáo định kỳ về tiến độ và mọi biến cố bất lợi. Khi nghiên cứu kết thúc, báo cáo kết quả cuối cùng phải được nộp đầy đủ để thẩm định. Một số báo cáo nghiên cứu đạt chất lượng tốt có thể được đăng tải trên các Tạp chí Y học uy tín.
Ứng dụng của nghiên cứu lâm sàng trong truyền thông và quảng cáo sản phẩm
Việc tham gia vào các nghiên cứu lâm sàng đòi hỏi nguồn lực khổng lồ về tài chính, nhân lực và tuân thủ các quy định nghiêm ngặt. Chính vì vậy, hầu hết các doanh nghiệp tham gia vào hoạt động nghiên cứu lâm sàng đều là những doanh nghiệp lớn có uy tin và trách nhiệm cao, tiềm lực mạnh, cam kết dài hạn với khoa học và chất lượng sản phẩm. Họ nhận thức rõ giá trị của bằng chứng khoa học trong việc xây dựng niềm tin với người tiêu dùng và khẳng định vị thế trên thị trường.
 |
Đặc biệt, kết quả từ các nghiên cứu lâm sàng có vai trò cực kỳ quan trọng trong hoạt động truyền thông. Chúng không chỉ là bằng chứng khoa học xác thực mà còn là cơ sở pháp lý vững chắc để doanh nghiệp khẳng định chất lượng và công dụng của sản phẩm theo đúng quy định của Nhà nước. Việc trích dẫn kết quả nghiên cứu lâm sàng trong các tài liệu quảng cáo, hướng dẫn sử dụng hay tư vấn sản phẩm giúp tăng cường tính thuyết phục, minh bạch và đảm bảo người tiêu dùng nhận được thông tin chính xác, đáng tin cậy, tránh những quảng cáo phóng đại hay thiếu cơ sở.
Tóm lại, nghiên cứu lâm sàng và thử nghiệm lâm sàng là những bước không thể thiếu từ các doanh nghiệp lớn có trách nhiệm với cộng đồng để đảm bảo rằng các sản phẩm y dược và dinh dưỡng được đưa ra thị trường đều an toàn, hiệu quả và có cơ sở khoa học vững chắc, góp phần nâng cao chất lượng chăm sóc sức khỏe cho cộng đồng.






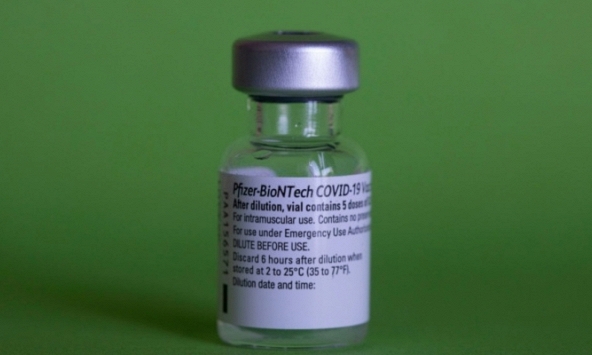






Pfizer và BioNTech bắt đầu thử nghiệm lâm sàng vaccine dành riêng cho biến thể Omicron
Pfizer và BioNTech bắt đầu thử nghiệm lâm sàng vaccine dành riêng cho biến thể Omicron
Pfizer và BioNTech bắt đầu thử nghiệm lâm sàng vaccine dành riêng cho biến thể Omicron
Pfizer và BioNTech bắt đầu thử nghiệm lâm sàng vaccine dành riêng cho biến thể Omicron
PGS.TS.BS Hoàng Thị Phượng, nhà khoa học đặc biệt say mê với điều trị lâm sàng.
Lần đầu tiên thử nghiệm lâm sàng thuốc tránh thai dành cho nam giới
Cùng chuyên mục
Thực phẩm siêu chế biến có thể âm thầm làm suy giảm khả năng tập trung của não bộ
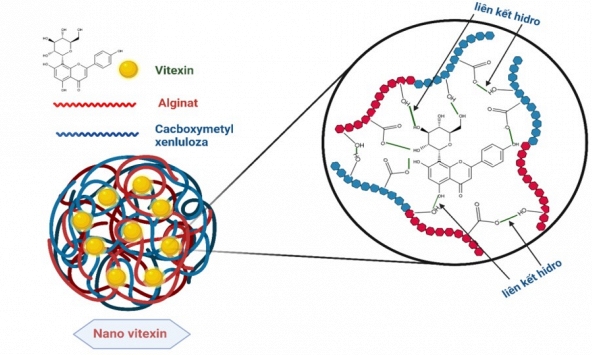
Nhóm nghiên cứu của TS. Ngô Thị Hoài Thu chế tạo thành công nanovitexin, mở hướng mới hỗ trợ điều trị đái tháo đường
Các nhà khoa học Nga nghiên cứu thành công virus biến đổi gene diệt ung thư, không gây hại mô lành
PGS.TS. Nguyễn Thị Xuân cùng nhóm nghiên cứu đột phá giải mã hệ gen tế bào gốc CD34+ trong ung thư hạch
Khi AI làm khoa học: Vai trò của nhà khoa học sẽ đi về đâu trong thập kỷ tới?
Ai Cập trồng thành công lúa mì bằng nước mặn