 |
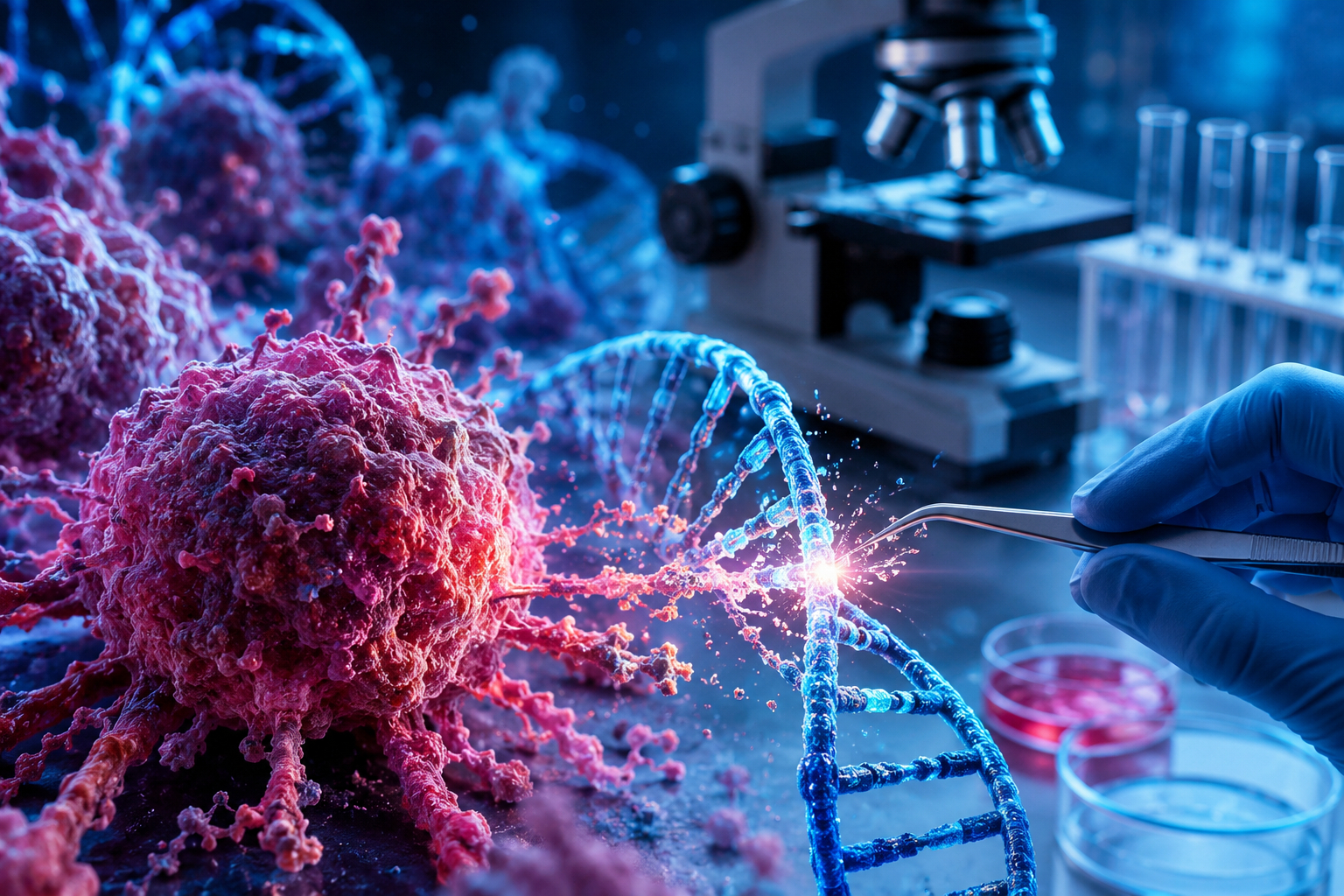
Nhóm nghiên cứu Hàn Quốc dẫn đầu bởi nhà khoa học Kyungjae Myung đến từ Viện Khoa học Cơ bản (IBS) phối hợp với Joo-Yong Lee (Đại học Chungnam) mới đây đã phát hiện một cơ chế mới có thể khiến những khối u đã kháng điều trị trở nên nhạy cảm trở lại với thuốc ung thư.
Trong cơ thể, các tế bào ung thư thường mang nhiều DNA bị tổn thương nhưng lại có thể tồn tại nhờ cơ chế tự sửa chữa hiệu quả. Một cơ chế phòng vệ then chốt là quá trình “tái tổ hợp tương đồng” (homologous recombination) có khả năng sửa chữa có độ chính xác cao, giúp khôi phục các đoạn DNA bị đứt gãy bằng sự hỗ trợ của các protein quan trọng như RAD51 và CHK1.
Nhiều liệu pháp điều trị ung thư hiện nay, điển hình là thuốc ức chế PARP trong liệu pháp điều trị đích, được thiết kế nhằm ngăn chặn quy trình này để tiêu diệt các tế bào ung thư. Tuy nhiên theo thời gian, nhiều khối u có thể phục hồi lại khả năng sửa chữa DNA, từ đó trở nên kháng thuốc và làm giảm hiệu quả điều trị.
Theo nhóm nghiên cứu, thay vì tác động trực tiếp vào đột biến gen, phương pháp mới nhắm tới việc phá vỡ sự ổn định của chính hệ thống sửa chữa DNA bên trong tế bào ung thư.
Thông qua phương pháp sàng lọc dựa trên tế bào nhằm nghiên cứu phản ứng trước áp lực sao chép DNA, các nhà khoa học đã xác định được phân tử nhỏ UNI418. Khi áp dụng vào các tế bào ung thư, nhóm nghiên cứu nhận thấy UNI418 làm giảm mạnh nồng độ của các protein sửa chữa DNA quan trọng như RAD51 và CHK1. Sự suy giảm này khiến tế bào ung thư mất khả năng sửa chữa DNA hiệu quả và trở nên dễ bị tổn thương hơn.
Đi sâu phân tích cơ chế hoạt động, các nhà khoa học phát hiện UNI418 làm kích hoạt một hệ thống phân hủy protein gọi là phức hợp ubiquitin ligase Cul4A. Hệ thống này có nhiệm vụ “đánh dấu” các protein mục tiêu để tế bào tiêu hủy chúng.
“Chúng tôi đã xác định được cơ chế khiến các protein sửa chữa DNA then chốt bị phân hủy chủ động ngay bên trong tế bào”, Giáo sư Joo-Yong Lee cho biết. Theo ông, đây là một cách hoàn toàn mới để kiểm soát quá trình tái tổ hợp tương đồng mà không cần can thiệp vào đột biến di truyền.
Ngoài ra, nghiên cứu cũng cho thấy UNI418 can thiệp vào con đường truyền tín hiệu liên quan đến chuyển hóa inositol phosphate, từ đó làm giảm nồng độ của phân tử IP6.
Trong điều kiện bình thường, IP6 có vai trò ức chế hoạt động của Cul4A. Khi lượng IP6 giảm xuống, cơ chế kìm hãm này bị loại bỏ, cho phép Cul4A hoạt động mạnh hơn. Kết hợp với protein điều hợp WDR5, Cul4A sẽ nhắm vào các protein sửa chữa DNA như RAD51 để phân hủy, khiến quá trình tái tổ hợp tương đồng bị ngừng lại hoàn toàn.
Theo các nhà nghiên cứu, cơ chế này tạo ra trạng thái tương tự như thiếu hụt khả năng sửa chữa DNA, ngay cả ở những tế bào ung thư vốn đã phục hồi chức năng sửa chữa trước đó. Hiệu ứng này đặc biệt quan trọng trong việc khắc phục tình trạng kháng thuốc ức chế PARP, một trong những thách thức lớn của điều trị ung thư hiện nay.
Trong các thử nghiệm trên tế bào ung thư, UNI418 giúp các tế bào trở nên nhạy cảm hơn với thuốc ức chế PARP. Phân tử này cũng phát huy tác dụng trên những dòng tế bào đã xuất hiện tình trạng kháng thuốc, giúp khôi phục khả năng đáp ứng điều trị.
Nhà khoa học Kyungjae Myung cho biết việc làm suy yếu hệ thống sửa chữa DNA có thể khiến các khối u kháng thuốc trở nên nhạy cảm trở lại với các liệu pháp hiện tại, từ đó mở ra chiến lược mới nhằm kéo dài hiệu quả của thuốc ức chế PARP.
Kết quả nghiên cứu tiếp tục cho hiệu quả khi thử nghiệm trên động vật. Trong các thí nghiệm ghép khối u ngoại lai, UNI418 giúp làm chậm đáng kể sự phát triển của khối u, đặc biệt khi kết hợp với thuốc ức chế PARP Olaparib.
Hiệu quả này vẫn được ghi nhận ở những dạng ung thư được thiết kế để mô phỏng tình trạng kháng thuốc.
Theo nhóm nghiên cứu, phát hiện mới này cho thấy ngay cả khi đã kháng điều trị, tế bào ung thư vẫn phụ thuộc mạnh vào hệ thống sửa chữa DNA để tồn tại. Việc phá vỡ sự ổn định của các protein sửa chữa DNA có thể làm lộ ra “điểm yếu” này và khiến khối u dễ bị tấn công trở lại.
Nghiên cứu cũng lần đầu cho thấy mối liên hệ trực tiếp giữa quá trình trao đổi chất của tế bào với cơ chế sửa chữa DNA thông qua tín hiệu IP6 và con đường phân hủy protein Cul4A.
Các nhà khoa học nhận định cơ chế mới này có thể trở thành nền tảng cho những liệu pháp phối hợp trong tương lai nhằm điều trị các loại ung thư đã kháng thuốc. Dù UNI418 vẫn cần thêm nhiều nghiên cứu trước khi có thể ứng dụng lâm sàng, kết quả hiện tại được đánh giá là bước tiến quan trọng trong cuộc chiến chống ung thư kháng điều trị.













Nghiên cứu giảm nguy cơ ung thư miệng bằng kẹo cao su
Hợp chất đường từ vi khuẩn dưới đáy Biển Đông khiến tế bào ung thư nổ tung
Công nghệ mới giúp đưa thuốc nhắm trúng tế bào ung thư, giảm tác dụng phụ
Nghiên cứu phương pháp mới trong điều trị ung thư ở phụ nữ
Nhật Bản thử nghiệm lâm sàng công nghệ tái tạo đồng thời xương và sụn khớp gối từ mô mỡ của người
Thử nghiệm thành công loại thuốc mới giúp kéo dài sự sống cho bệnh nhân ung thư tuyến tụy
Cùng chuyên mục
Phát hiện mới mở ra hy vọng điều trị cho bệnh nhân ung thư kháng thuốc
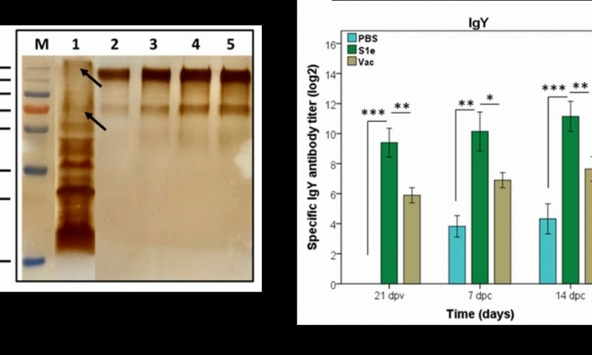
Sản xuất kháng nguyên từ thực vật: Hướng đi mới trong phát triển vaccine cho ngành chăn nuôi
Việt Nam lần đầu xây dựng cơ sở dữ liệu DNA cho sinh vật biển
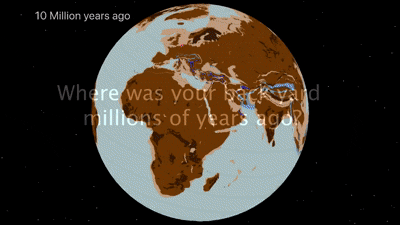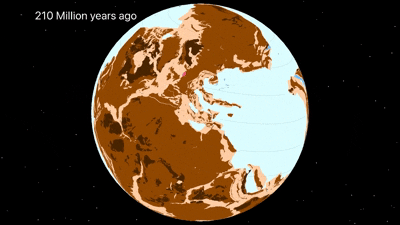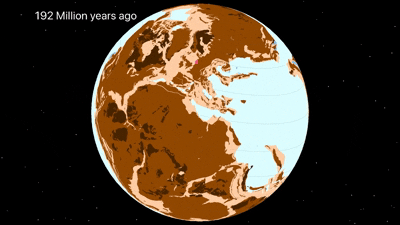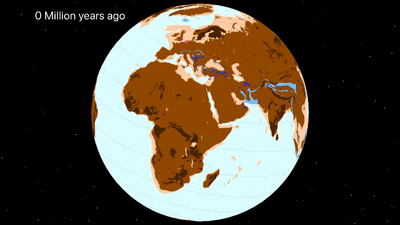
Công cụ trực tuyến giúp truy ngược vị trí trên Trái đất 320 triệu năm trước
Du lịch có thể góp phần làm chậm lão hóa và cải thiện sức khỏe tổng thể
Công nghệ Trung Quốc chuyển hướng sang trải nghiệm cảm xúc